Télécharger le document suivant à compléter comme support de cours et questions : C51_cours_mole
Définition de la mole
La définition de la mole1, unité de mesure des quantités de matière du Système International, date de 1971 soit il y a seulement 50 ans ! Le nombre d’entités (atomes, molécules, ions, électrons, etc.) contenues dans une mole est connue sous le nom de constante d’Avogadro, noté NA : $$N_A=6,02214129\times10^{23} mol^{-1}$$
Cette constante, d’importance fondamentale en chimie, permet de faire le lien entre la matière à l’état microscopique et à l’état macroscopique.
Sa découverte est liée à l’acceptation du modèle atomique par la communauté scientifique, et à l’étude des gaz moléculaires. Le chimiste Amedeo Avogadro (1776-1856) a grandement contribué à l’un (modèle atomique) et à l’autre (étude des gaz), mais n’a pas énoncé l’existance de cette constante d’Avogadro.
Contribution d’Avogadro à la chimie du XIXème siècle
Pour la majorité des chimistes du début du XIXème siècle, l’existence d’atomes semble être une idée complètement farfelue. Il y a, dans la communauté scientifique, une grande difficulté à distinguer un corps simple (comme O2) d’un corps composé (comme H2O). Et l’exploration de la matière ne permet pas de déterminer que le corps simple O2 est constitué de molécules, où 2 atomes d’oxygène sont liés par une liaison covalente.
En 1810, Avogadro énonce dans son ouvrage New System of Chemical Philosophy, la loi des proportions multiples :
Il admet que la matière à l’état gazeux est constituée de molécules, mettant par exemple les atomes A et B en combinaisons de type AB, AB2, A2B, …etc. Il admet également que le nombre de ces molécules, dans un volume V de gaz, à la température T, est le même, quel que soit la nature du gaz2.
Il publie ensuite ses recherches sur la relation entre les masses de différents gaz 3, pris dans les mêmes conditions de Volume et Temperature. Le rapport des masses de gaz est alors supposé identique au rapport des masses des molécules constituantes. Cela lui permet, finalement, de définir :
- l’hypothèse de l’existence des molécules
- les formules moléculaires de ces gaz
- les rapports des masses atomiques pour les constituants de ces gaz : l’oxygène est par exemple 16 fois plus lourd que l’hydrogène, élément le plus leger.
Ainsi, en prenant une valeur de masse atomique égale à 1 pour l’hydrogène :
- la molécule H2O, constitué de 2 atomes de H et un atome O aura une masse égale à 1 + 1 + 16 = 18 fois la masse d’un atome H.
- la molécule de dihydrogène H2 a une masse égale à 1 + 1 = 2.
- le rapport des masses de ces 2 gaz serait alors égal à 18/2, donc 9.
L’echelle macroscopique
On a vu dans le cours précédent (échanges thermique : Les atomes et molécules ont un mouvement d’agitation). Leur énergie de mouvement est proportionnelle à leur température.
agitation à l'echelle atomique
La température est une grandeur macroscopique

Exercice resolu
Enoncé
Un gaz contenant x mol d’ammoniac, de formule NH3 pèse 2,55g. Un autre gaz, contenant autant de moles que le premier gaz, et constitué de dioxygène O2, pèse 4,8g.
Calculer la masse molaire de l’azote N, en supposant que celle de H vaut 1, et celle de O vaut 16.
Réponse
En adoptant la démarche d’Avogadro, on peut :
-
calculer le rapport des masses de ces 2 gaz : $$r = \tfrac{2,55}{4,8}$$
-
puis exprimer la masse d’une mole de NH3 en fonction de celle de N et celle de H : La masse d’une molécule étant calculée en faisant la somme des masses des atomes qui la constituent, on a :
$$m_{NH3} = m_N + 3 \times m_H$$
$$m_{NH3} = m_N + 3 \times 1$$
- et la masse d’une mole de O2 en fonction de celle de O : $$m_{O2} = 2 \times m_O$$
$$m_{O2} = 2 \times 16$$
$$m_{O2} = 32$$
- enfin, exprimer le rapport des masses de ces 2 produits gazeux et résoudre. Comme les 2 gaz contiennent le même nombre de molécules, le rapport des masses des 2 gaz est égal au rapport des masses des 2 types de molécules. On a alors :
$$r = \tfrac{m_{NH3}}{O2}$$
$$\tfrac{2,55}{4,8} = \tfrac{m_N + 3}{32}$$
La résolution de cette équation à une inconnue donne alors m = 14 pour l’azote. Ce qui signifie qu’une mole d’atomes d’azote est 14 fois plus lourde qu’une mole d’atomes d’hydrogène.
Des unités de quantité de matière
quelques repères
Ce concept d’unité de quantité de matière vous est déjà familier : il arrive que l’on rassemble les objets par paquets de dimension fixe :
- La paire contient ainsi : 2 objets
- La douzaine contient : 12 objets
- …
- La mole contient : 6,02.1023 objets
dénombrer les objets par paquets
n paires
Vous avez n = 20 paires de chaussures dans votre placard. Cela signifie que vous possédez :
$$N = n \times 2$$
Soit N = 40 chaussures. Cette relation pourrait aussi s’exprimer sous la forme :
$$n = \tfrac{N}{2}$$
n douzaines
Une bouriche de N = 66 huitres contient n douzaines, que l’on peut calculer avec la relation :
$$n = \tfrac{N}{12}$$
$$n = \tfrac{66}{12}$$
$$n=5,5 \quad douzaines$$
n moles
Un échantillon de N = 1021 atomes contient un nombre n de mol, tel que :
$$n = \tfrac{N}{N_A}$$
$$n = \tfrac{10^{21}}{6,02\times 10^{23}}$$
$$n=1,66.10^{-3}mol$$
Dénombrer avec la masse molaire
masse molaire
C’est la masse d’une mole d’objets. On la note M (majuscule). La masse molaire atomique est indiquée dans le tableau périodique des éléments voir en bas de page
Exemples :
- La masse d’une mole d’atomes d’oxygène vaut M = 16 g
- La masse d’une mole de dioxygène vaut M = 2*16 = 32 g
méthode
si 1 mole d’objet pèse M : alors n mol d’objet pèse m.
On peut représenter ces grandeurs de la manière suivante :
| 1 | M |
|---|---|
| n | m |
On a alors la relation :
$$n = \tfrac{m}{M}$$
application
On a vu que la masse molaire de O2 vaut M = 32 g. Si on dispose d’un échantillon gazeux de masse m = 1,8 g de O2, alors on peut évaluer le nombre de moles qu’il contient :
$$n = \tfrac{m}{M}$$
$$n = \tfrac{1,8}{32}$$
$$n = 5,2.10^{-2}mol$$
$$n = \tfrac{N}{N_A}$$
où N<sub>A</sub> représente le nombre d'Avogadro.<br>
Cette manière de compter les entités, en mole(s) n'est adaptée que pour des entités à l'échelle microscopique : atomes, ions, molécules, électrons.
</li>
<li>La définition historique de la mole :<br>C'est le nombre d'atomes isotopes du carbone <sup>12</sup>C dans un échantillon de masse 12,0g.<br>En d'autres termes, une mole d'hydrogène <sup>1</sup>H pèse 1,0g, une mole de <sup>16</sup>O pèse ... 16,0g. Ce nombre est ajusté pour avoir cette correpondance entre le nombre de masse et la masse d'une mole du même isotope.</li>
<li>Quantité de matière :<br>On appelle quantité de matière le nombre de moles constituant l'échantillon. On note cette quantité avec la lettre n. Son unité, mole(s), peut se noter de manière raccourcie mol.
$$n = \tfrac{m(ech)}{M(atome)}$$
</li>
Liens
- Avogadro : sa constante : entre mythe et réalité http://culturesciences.chimie.ens.fr/
tableau périodique réduit des éléments
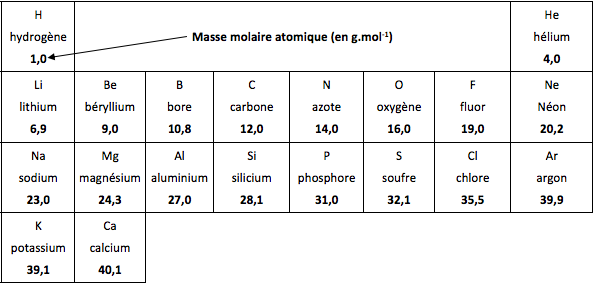
masses molaires atomiques
-
La mole est la quantité de matière d’un système contenant autant d’entités élémentaires qu’il y a d’atomes dans 0,012 kilogrammes de carbone 12 ↩︎
-
c’est l’énoncé de la loi d’Avogadro : Le nombre de molécules contenues dans un volume V et à la température T est indépendant du type de gaz. Il y a forcément le même « vide » entre les particules donc le même nombre d’espèces dans un même volume. ↩︎
-
Avogadro (1811) : Essai d’une manière de déterminer les masses relatives des molécules élémentaires des corps et les proportions selon lesquelles elles entrent dans les combinaisons ↩︎
