Spectres de raies : la lampes spectrales
Introduction : l’atome de Bohr
Niels Bohr, physicien danois, formule en 1913 l’hypothèse que les atomes occupent des niveaux d’énergie bien déteminés. Son modèle atomique est adapté à l’atome d’hydrogène. Mais il sera aussi adapté aux autres atomes avec des enrichissements venant de la théorie quantique (Hamilton).
Cette énergie est liée à l’interaction entre le noyau de l’atome et son électron. Elle dépend de la position de l’électron, sur des niveaux électroniques (les orbitales) qui vont du plus près (niveau n=1) au plus loin de l’atome (niveau n=7).
L’électron occupe préférentiellement l’orbitale de plus basse énergie (n=1). Lorsque l’électron change d’orbitale (de niveau d’énergie), on dit qu’il y a une transition électronique.
Une transitions électronique vers un niveau inférieur peut s’accompagner d’une emission d’une particule de lumière (un photon). La video suivante explique ceci plus en détail :
L’animation : lampe à décharge (utilise java)
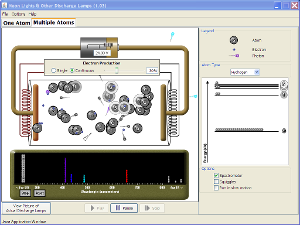
L’expérience suivante simule une lampe à décharge : avec une tension suffisante, délivrée par une pile, des électrons sont émis dans un tube depuis l’électrode (-) vers l’électrode (+). Sur leur passage, ils rencontrent un atome constitutif du gaz de ce gaz. L’énergie du choc est absorbée par l’atome. Son électron passe alors du niveau fondamental (n=1) vers un niveau supérieur. Puis, après un certain temps, il revient vers son niveau fondamental, directement, ou avec des étapes à des niveaux intermédiaires (par exemple 3 -> 2 puis 3 ->1). Il se produit une ou plusieurs transitions électroniques, avec émission de photons.
Ces transitions sont représentées sur le diagramme d’énergie, à droite. Chaque plateau horizontal est un niveau d’énergie, occupé ou non par l’électron.
Le spectrophotomètre mesure le nombre de photons émis pour chaque longueur d’onde.
Travail
Cocher les paramètres : spectromètre, gribouillis, passer au ralenti
- Légender le schéma fourni avec : électrode (-), électrode (+), pile, atome, électron, photon, diagramme d’énergie, fenêtre du spectrophotomètre, transition électronique
- Que signifie le numéro inscrit sur l’atome de gaz, au milieu du tube ?
- Les électrons qui percutent l’atome, sont ils ralentis par le choc ? Si oui, dans quel cas ?
- Combien de photons sont émis lors d’un choc entre électron et atome ?
- Comment soit être réglée la tension de polarisation des électrodes pour que les photons émis soient tous de couleur rouge ?
- Régler la pile pour avoir des photons de différentes couleurs. Attendre suffisament longtemps pour que le spectrophotomètre indique un certain nombre de radiations émises. Relever les valeurs des longueurs d’ondes des photons émis.
- Utiliser le lien suivant pour repérer quelles transitions sont responsables de l’émission des photons du domaine du visible. (de quel niveau, et vers quel niveau électronique)
- Comment s’appelle cette série de transition avec emission dans le visible : Lyman, Balmer, Paschen, Brakett, Plund ?